リチウムイオン電池の内部で、リチウムイオンが電解液を介して正極~負極間を行き来することで充放電が行われます。
正極材料には、一般的にコバルト、ニッケル、マンガンの単一または複合の金属酸化物やLiFePO4のようなリン酸鉄系の材料が使用されます。
負極材料には、一般的に炭素系材料や合金系の材料が使用されます。
下記図は、金属酸化物と炭素を例に取った充放電の模式図です。
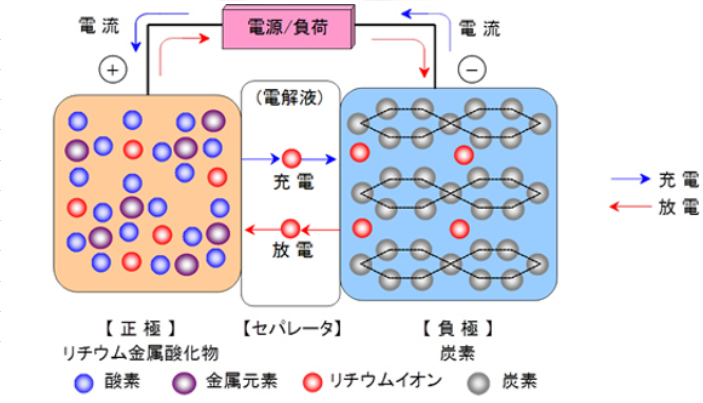
図.リチウムイオン電池の原理の模式図(一例)
充電反応
外部の充電電源により、電流の移動にともなって正極の結晶構造からリチウムイオンが電解液中に抜け出し、負極の炭素結晶層間に挿入されます。
放電反応
負極の炭素結晶層間からリチウムイオンが電解液中に抜け出し、正極の結晶構造に挿入されることで、外部回路に電流が取り出せ、負荷に仕事をさせることができます。
反応式(一般的な例)
正極では、 Li(1-x)MO2 + xLi+ + xe- ←→ LiMO2
M:金属元素(例:Ni、Mn、Co)
負極では、LixC ←→ C + xLi+ + xe-
電池全体としては、
Li(1-x)MO2 + LixC ←→ LiMO2 + C
となります。
